行業(yè)動態(tài)
您當前的位置 > 行業(yè)動態(tài) > 行業(yè)法規(guī)
國家藥監(jiān)局發(fā)文,14品種迎大利好
加入日期:2019/1/3 9:05:03 查看人數(shù): 1204 作者:admin
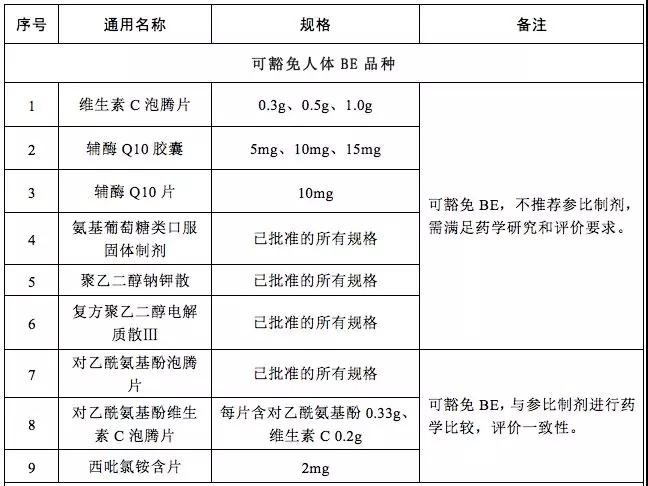
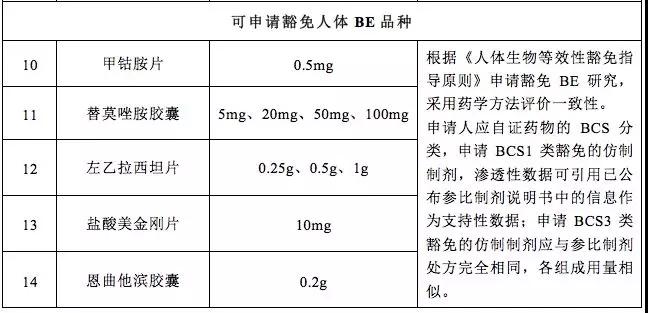
12月29日,國家藥監(jiān)局官網(wǎng)發(fā)布《國家藥品監(jiān)督管理局關于發(fā)布可豁免或簡化人體生物等效性(BE)試驗品種(第二批)的通告(2018年第136號)》,有9個品種可豁免人體BE,5個品種可申請豁免人體BE。

28日,國家藥監(jiān)局才正式發(fā)文,確定一致性評價年末大限延期,今天又傳來好消息,14個品種可豁免BE。
此前,全國人大代表、亞寶藥業(yè)董事長任武賢在接受媒體采訪時表示,對于2018年底前完成一致性評價,這個實施的壓力非常大。
雖然現(xiàn)在對于“289基藥目錄”的品種來說,大限延期,壓力緩解了,但是,資金方面的壓力仍不能忽略。
對此,任武賢也曾對媒體表示,原來做一致性評價的成本是50-60萬元,如今對此的技術要求更高了,一致性評價剛開始,300萬是人情價,如果正式開始以后,一致性評價將來的價格將在500萬以上,這樣這個投入是很大的。再加上前期基礎研究的成本,一個產品下來沒有800萬左右是出不來。
此前,有研究人員曾公開表示,由于生物等效性試驗會耗費大量人力、財力和時間,它增加了研究者的研發(fā)成本,延長了申請人的注冊周期,延緩了產品上市銷售速度。盡快開展和接受生物豁免,以提高新藥研發(fā)、仿制藥開發(fā)和一致性評價的效率是"箭在弦上"。
如今,能夠豁免BE,這對于相關企業(yè)來無疑是天大的好消息。如果符合目錄的品種在做一致性評價的時候,只要溶出曲線一致即可,這相比生物等效性試驗而言,藥企將省下了不少成本費用。
附:可豁免或簡化人體生物等效性(BE)試驗品種(第二批)